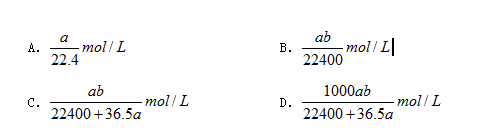║║║║1.тзхща©ф©ио÷oпХсп≤к(bi╗║o)с⌡╣дйг
║║║║A.≤к(bi╗║o)╬─ B.°ь╤х C.²Б╤х D.хща©
║║║║2.дЁ▄█(sh╗╙)Р·(y╗╓n)пХр╙0.2 mol NaOH╧лСwё╛сцмп╠PлЛф╫╥Qх║╧лСw∙r(sh╗╙)ё╛лЛф╫вx■╣(sh╗╢)(сн╢a╪╟Мю╢a)▄╒
║║║║A.╣хсз8.0g B.╣хсз8.00g
║║║║C.╢Ссз8.0g D.╣хсз0.2g
║║║║3.0.5L 1mol/L╣дFeCl3хэр╨еc0.2L 1 mol/L╣дKClхэр╨жп��ё╛Cl-²Б╤х╠х·И
║║║║A.15║ц2 B.1║ц1 C.3║ц1 D.1║ц3
║║║║4.оЮ▄╕(du╗╛)╥жвсы|(zh╗╛)а©·ИM╣ддЁнОы|(zh╗╛)тзйр°ьоб╣дхэ╫Б╤х·ИS g���ё╛╢к∙r(sh╗╙)°y(c╗╗)╣цО√╨мхэр╨╣дцэ╤х·И╕яg║╓cm-3���ё╛└tт⌠О√╨мхэр╨╣днОы|(zh╗╛)╣да©²Б╤хйг

║║║║5.▄╒≤к(bi╗║o)°й(zh╗Ёn)═Н⌡rоб╣дa L HCl( Б)хэсз1000gк╝жпё╛╣ц╣╫╣дШ}кАцэ╤х·Иb g/cm3ё╛└tт⌠Ш}кА╣днОы|(zh╗╛)╣да©²Б╤хйг
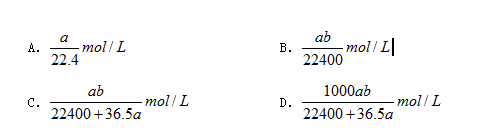
║║║║6.NA·И╟╒╥Э╪с╣ба_Ёё■╣(sh╗╢)����ё╛обапЙP(gu╗║n)сз0.2mol/L K2SO4хэр╨╣дуЩ╢_уf╥╗йг
║║║║A.500mLхэр╨жпкЫ╨╛K+║╒SO42-©┌■╣(sh╗╢)·И0.3NA
║║║║B.500mLхэр╨жп╨╛сп0.1NA┌─(g╗╗)K+Кxвс
║║║║C.1Lхэр╨жпK+Кxвс²Б╤хйг0.2mol/L
║║║║D.2Lхэр╨жпSO42-Кxвс²Б╤хйг0.4mol/L
║║║║7.х║100mL 0.3mol/L╨м300mL 0.25mol/L╣даРкАв╒хК500mLхща©ф©жп�����ё╛╪ск╝о║А▄жа©л╤х╬─�����ё╛т⌠╩Л╨охэр╨жпH+╣днОы|(zh╗╛)╣да©²Б╤хйг
║║║║A.0.21mol/L B.0.42mol/L
║║║║C.0.56mol/L D.0.26mol/L
║║║║8.дЁAl2(SO4)3хэр╨V mLжп╨╛a g Al3+�ё╛х║ЁЖV/4 mLхэр╨о║А▄Ёи4V mL╨Сё╛SO42-╣днОы|(zh╗╛)╣да©²Б╤х·И
║║║║A.125/54V mol║╓L-1 B.125a/36V mol║╓L-1
║║║║C.125a/18V mol║╓L-1 D.125a/V mol║╓L-1
║║║║9.▄╒2.4molдЁ╫П▄ым╤хК1.8L 2mol/L╣ддЁкАхэр╨жп��ё╛г║╨цмЙх╚╥╢▒╙(y╗╘ng)�����ё╛╡╒╝a(ch╗ёn)иЗ7.2g Д Б��ё╛└tт⌠╫П▄ы╨мкА╥ж└eйг
║║║║A.╤Ч┐r(ji╗╓)╫П▄ы��ё╛╤Чт╙кА
║║║║B.╤Ч┐r(ji╗╓)╫П▄ы����ё╛хЩт╙кА
║║║║C.хЩ┐r(ji╗╓)╫П▄ы���ё╛╤Чт╙кА
║║║║D.р╩┐r(ji╗╓)╫П▄ыё╛р╩т╙кА
║║║║10.еДжфр╩╤╗Сw╥e�����║╒р╩╤╗нОы|(zh╗╛)╣да©²Б╤х╣дхэр╨�ё╛▄█(sh╗╙)Р·(y╗╓n)╫Y(ji╗╕)╧Ш╝a(ch╗ёn)иЗф╚╣мс╟М▒╣дйг
║║║║A.хща©ф©жпт╜спиыа©уТПsк╝
║║║║B.хэ╫БкЫсц╣д÷Щ╠╜н╢о╢°Л
║║║║C.╤╗хщ∙r(sh╗╙)яЖр∙с^╡Лр╨цФ
║║║║D.╤╗хщ∙r(sh╗╙)╦╘р∙с^╡Лр╨цФ
║║║║11.спK2SO4╨мAl2(SO4)3╣д╩Л╨охэр╨ё╛ряж╙фДжпAl3+╣днОы|(zh╗╛)╣да©²Б╤х·И0.4mol/L��ё╛SO42-╣днОы|(zh╗╛)╣да©²Б╤х·И0.7mol/L�ё╛└t╢кхэр╨жпK+╣днОы|(zh╗╛)╣да©²Б╤х·И
║║║║A.0.1mol/L B.0.15mol/L
║║║║C.0.2mol/L D.0.25mol/L
║║║║12.тз100g²Б╤х·И18mol/L║╒цэ╤х·И╕я╣д²БаРкАжп╪схКр╩╤╗а©╣дк╝о║А▄Ёи9mol/L╣даРкА��ё╛└t╪схКк╝╣дСw╥e
║║║║A.п║сз100mL B.╣хсз100mL
║║║║C.╢Ссз100mL D.╣хсз100/P.ML
║║║║13.сццэ╤х·И1.32g/cm3╣даРкАхэр╨жП╣н╣нхК╣╫BaCl2хэр╨жп����ё╛ж╠╣╫Ёа╣Мг║╨цмЙх╚·Иж╧║ёряж╙кЫиЗЁи╣дхэр╨╣ды|(zh╗╛)а©╣хсзт╜BaCl2хэр╨╣ды|(zh╗╛)а©���ё╛└tH2SO4хэр╨╣д²Б╤х·И
║║║║A.21.9% B.42.1%
║║║║C.13.5mol/L D.5.67mol/L
║║║║14.ы|(zh╗╛)а©·И8.02g╣дХFф╛ё╛╥еъM(j╗╛n)1.0L 0.90mol/L╣дCuSO4хэр╨жп�ё╛ъ^р╩╤н∙r(sh╗╙)Иgх║ЁЖо╢┐Т�║╒╦итО�����║╒╥Qа©�����ё╛ы|(zh╗╛)а©·И8.66g�����║ёхТуJ(r╗╗n)·Ихэр╨╣дСw╥e⌡]спв┐╩╞��ё╛└tCu2+╣д²Б╤хв┐?y╗╜u)?/P>
║║║║A.0.89mol/L B.0.82mol/L
║║║║C.0.78mol/L D.0.6mol/L
║║║║15.▄╒4gNaOHхэ╫Бтз10mLк╝жп�����ё╛о║жа1L╨Сх║ЁЖ10mL�ё╛фДнОы|(zh╗╛)╣да©²Б╤хйг
║║║║A. 1mol/L B. 0.1mol/L
║║║║C. 0.01mol/L D. 10mol/L